¿Alguna vez te has preguntado por qué algunos elementos reaccionan... Prikaži više
Tendencias y Propiedades en la Tabla Periódica






Introducción a las Propiedades Periódicas
Las propiedades periódicas son las características de los elementos que varían de forma predecible en la tabla periódica. Esta periodicidad se debe a cómo se repiten las configuraciones electrónicas de la capa de valencia.
Hay dos conceptos clave que explican todo: la carga nuclear efectiva es la carga positiva "real" que siente un electrón de valencia. No es igual al número atómico porque los electrones internos "apantallan" parte de esa carga.
En un periodo (→): Z_ef aumenta porque hay más protones pero los electrones van a la misma capa. En un grupo (↓): Z_ef se mantiene casi constante para la última capa porque aunque hay más protones, también hay más capas internas que apantallan.
¡Dato clave! El efecto pantalla es como un escudo: los electrones internos protegen a los de valencia de la atracción total del núcleo.

Radio Atómico
El radio atómico es la mitad de la distancia entre núcleos de dos átomos idénticos enlazados. Es como medir el "tamaño" de un átomo.
En un grupo (↓): aumenta porque se añaden nuevas capas electrónicas. Cada capa nueva está más lejos del núcleo, así que el átomo es más grande. En un periodo (→): disminuye porque aunque el número de capas es el mismo, la Z_ef aumenta y "tira" más fuerte de los electrones, contrayendo el átomo.
Piénsalo así: es como si el núcleo fuera un imán que se hace más fuerte hacia la derecha (mismo periodo) pero más débil hacia abajo (mismo grupo) debido a la distancia.
Truco para recordar: Los átomos más grandes están en la esquina inferior izquierda, los más pequeños en la superior derecha.

Radio Iónico
Cuando un átomo gana o pierde electrones, su tamaño cambia drásticamente. Los cationes (iones positivos) son más pequeños que el átomo neutro porque al perder electrones, a menudo se pierde toda la capa de valencia y los restantes son atraídos con más fuerza.
Los aniones (iones negativos) son más grandes que el átomo neutro. Al ganar electrones en la misma capa, aumenta la repulsión entre ellos y la nube electrónica se expande.
Para especies isoelectrónicas (mismo número de electrones), a más protones en el núcleo, menor radio. Es lógico: más "tirón" hacia el centro.
Regla fácil: Perder electrones = encogerse, ganar electrones = hincharse.

Energía de Ionización
La energía de ionización (EI) es la energía necesaria para "arrancar" un electrón de un átomo gaseoso. Es como la fuerza que necesitas para separar algo que está pegado.
En un grupo (↓): disminuye porque los electrones están más lejos y más apantallados. En un periodo (→): aumenta porque la Z_ef aumenta y los electrones están más "pegados" al núcleo.
¡Cuidado con las excepciones! Grupo 2 vs. 13: El grupo 13 tiene EI menor porque es más fácil quitar un electrón p que uno de un orbital s completo. Grupo 15 vs. 16: El grupo 16 tiene EI menor porque elimina la repulsión de electrones emparejados.
Para examen: Aprende las excepciones de memoria. Be > B y N > O son preguntas típicas.

Afinidad Electrónica y Electronegatividad
La afinidad electrónica (AE) mide cuánto "le gusta" a un átomo aceptar un electrón. Si es muy negativa, significa que libera mucha energía al aceptarlo (es favorable).
En un grupo (↓): menos negativa (menos favorable) porque el electrón entrante está más lejos del núcleo. En un periodo (→): más negativa (más favorable) porque la Z_ef aumenta.
La electronegatividad es la capacidad de atraer electrones en un enlace. El flúor es el más electronegativo (4.0 en la escala de Pauling). Sigue las mismas tendencias: aumenta hacia la derecha y hacia arriba.
Dato importante: Los gases nobles tienen AE positiva - ¡no quieren electrones extra!
Ejemplos y Casos Prácticos
Para ordenar por radio atómico creciente: P, Cl, Na, Al (todos del periodo 3), aplicamos que el radio disminuye hacia la derecha. Resultado: Cl < P < Al < Na.
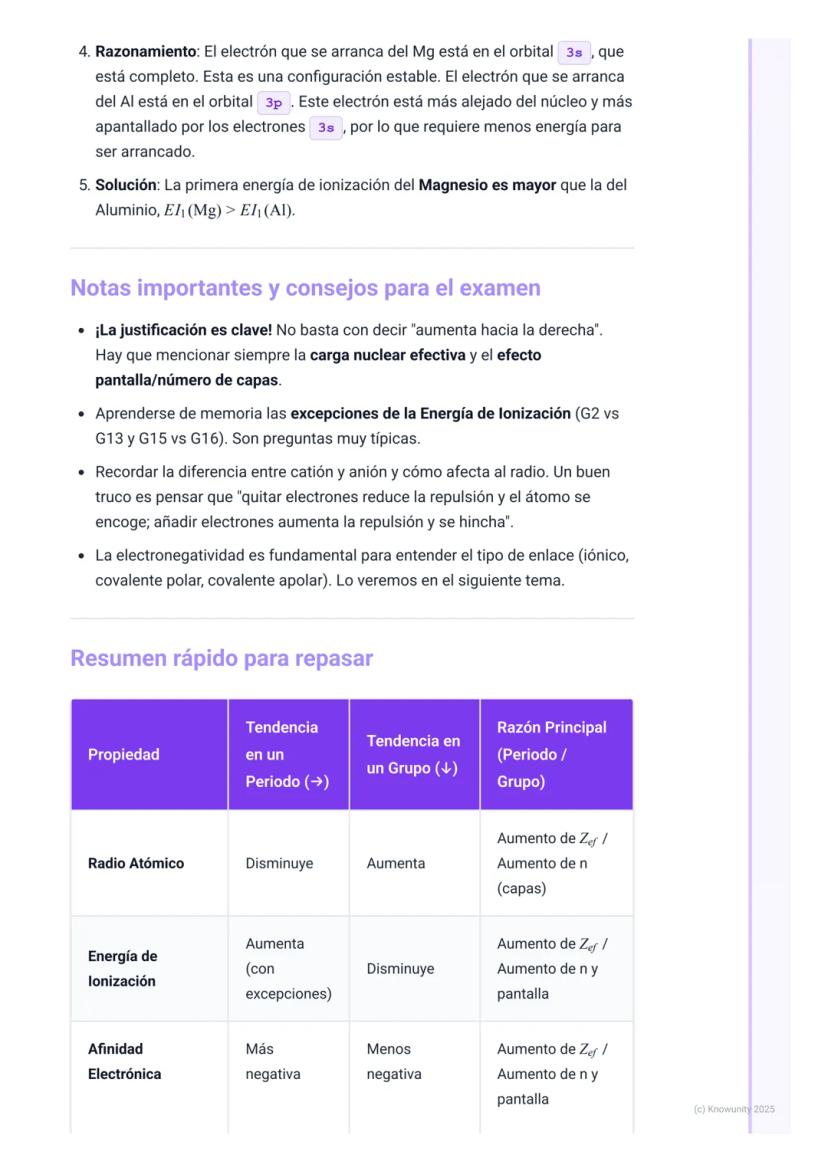
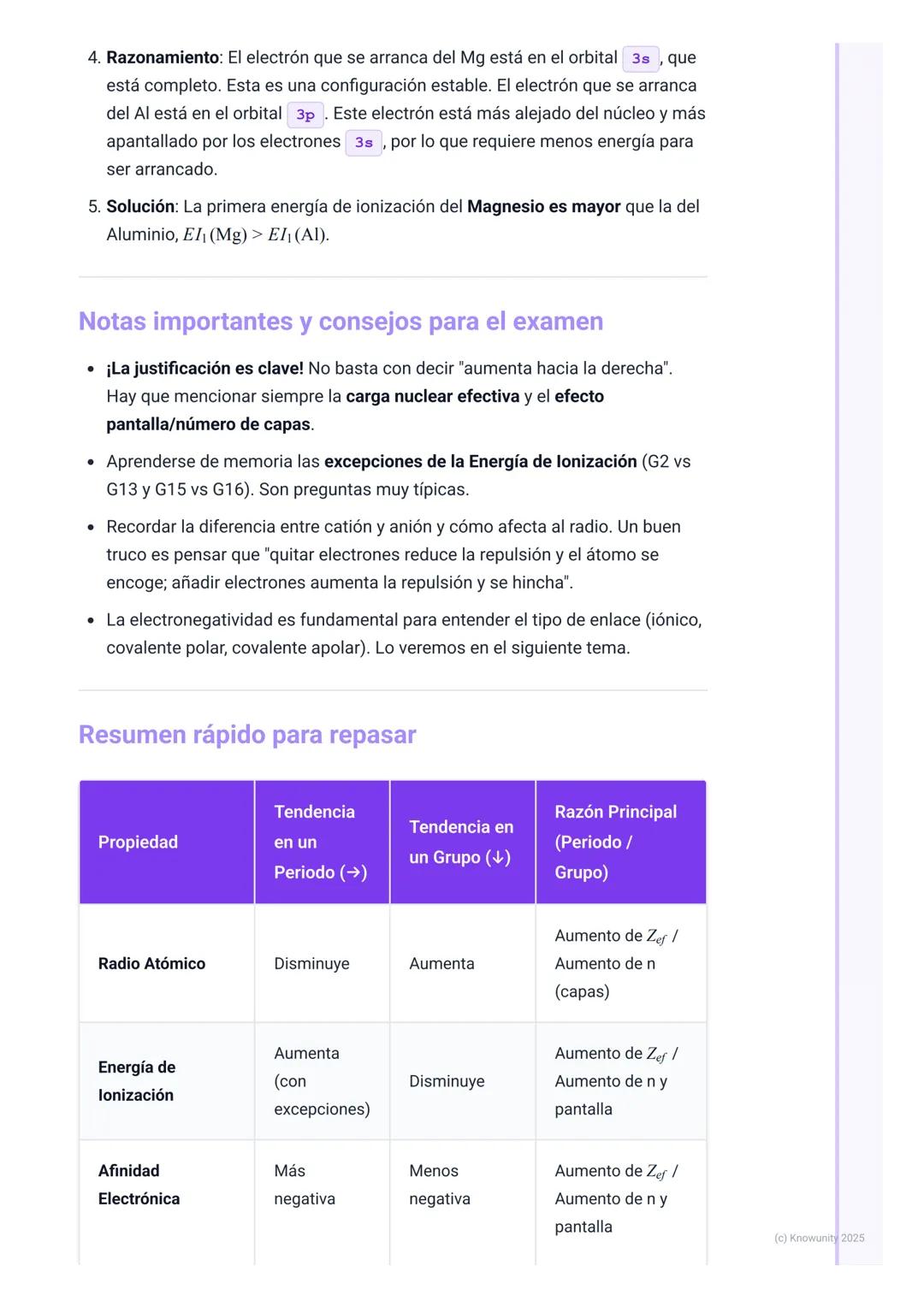
Para comparar energías de ionización entre Mg y Al, aunque Al está más a la derecha, EI(Mg) > EI(Al) por la excepción del grupo 2 vs. 13. El electrón 3p del Al es más fácil de arrancar que el 3s del Mg.
Las especies isoelectrónicas como O²⁻, F⁻, Ne, Na⁺, Mg²⁺ se ordenan por número de protones: a más protones, menor radio.
Clave del éxito: En el examen, siempre justifica con Z_ef y apantallamiento, no solo digas "aumenta hacia la derecha".
Resumen para Repasar
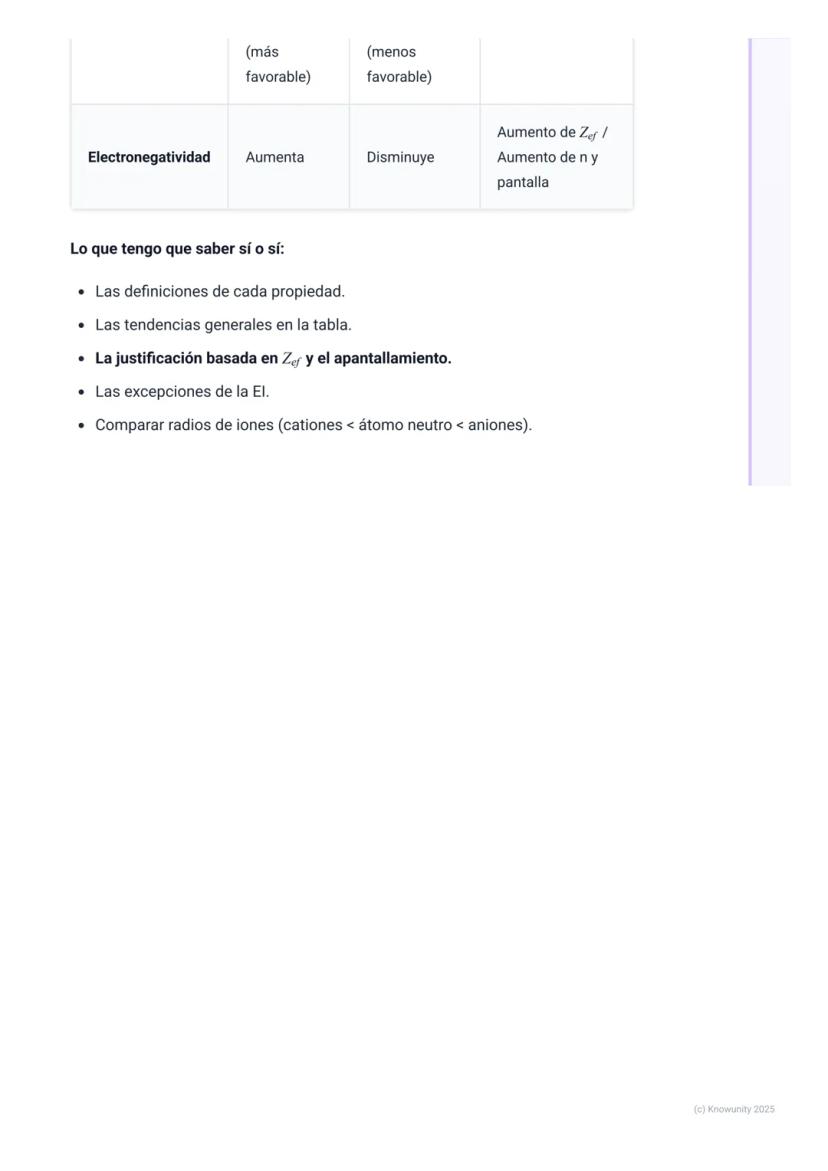
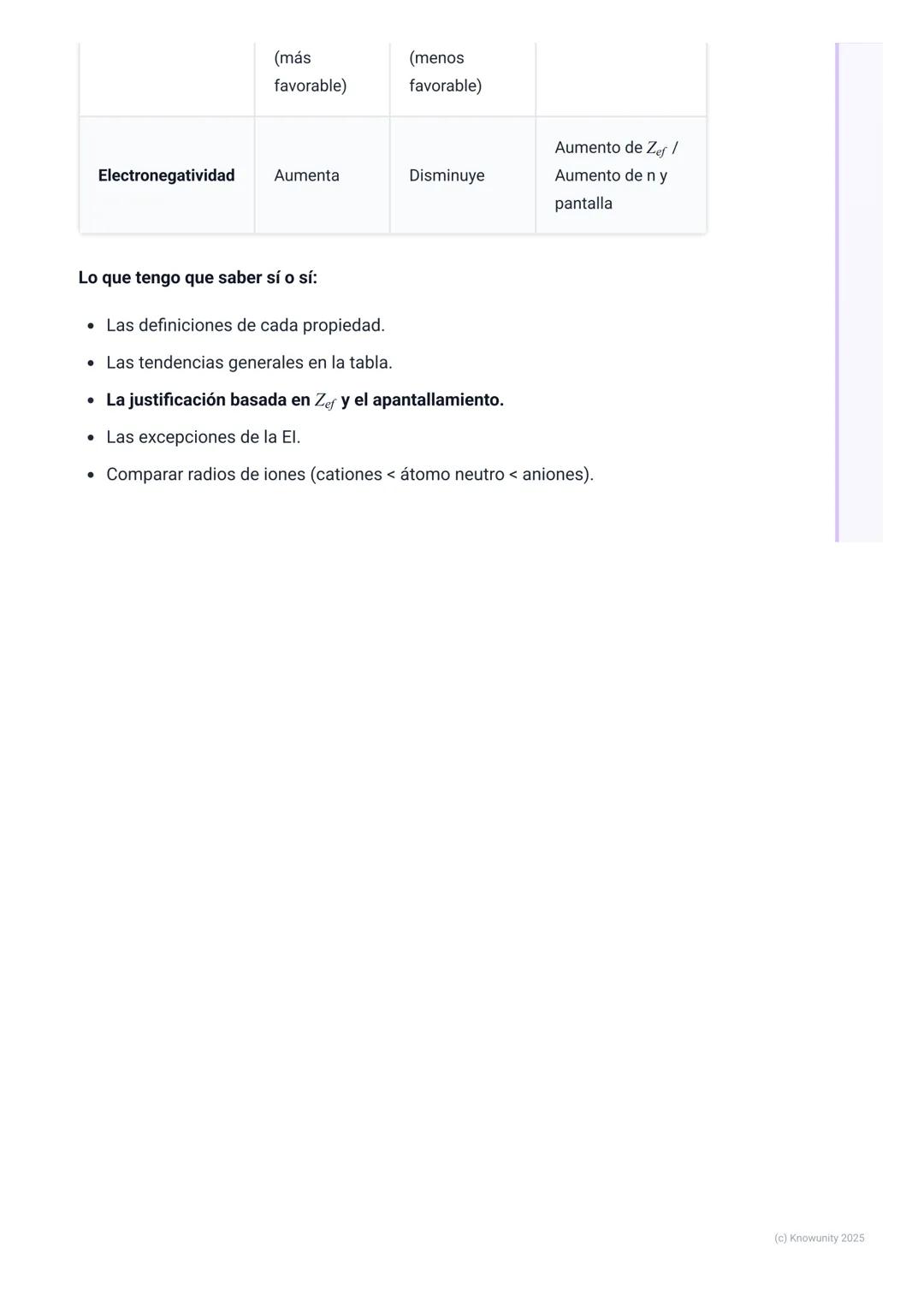
| Propiedad | Periodo (→) | Grupo (↓) | Razón |
|---|---|---|---|
| **Radio atómico** | Disminuye | Aumenta | Z_ef vs. capas nuevas |
| **Energía ionización** | Aumenta* | Disminuye | Z_ef vs. distancia+pantalla |
| **Afinidad electrónica** | Más negativa | Menos negativa | Z_ef vs. distancia+pantalla |
| **Electronegatividad** | Aumenta | Disminuye | Z_ef vs. distancia+pantalla |
*Con excepciones importantes
Lo esencial para el examen: definiciones, tendencias generales, justificaciones con Z_ef, excepciones de EI (G2 vs G13, G15 vs G16), y comparación de radios iónicos.
Consejo final: Practica con ejemplos hasta que puedas predecir propiedades sin mirar la tabla. ¡Es como tener superpoderes químicos!
Mislili smo da nikad nećeš pitati...
Šta je Knowunity AI companion?
Naš AI Companion je AI alat fokusiran na učenike koji nudi više od samih odgovora. Napravljen na milionima Knowunity resursa, pruža relevantne informacije, personalizovane planove učenja, kvizove i sadržaj direktno u chatu, prilagođavajući se tvom individualnom putu učenja.
Gde mogu da preuzmem Knowunity aplikaciju?
Možeš preuzeti aplikaciju sa Google Play Store-a i Apple App Store-a.
Da li je Knowunity stvarno besplatan?
Tako je! Uživaj u besplatnom pristupu sadržaju za učenje, povezuj se sa drugim učenicima i dobijaj trenutnu pomoć – sve na dohvat ruke.
Najpopularniji sadržaj u Química
9Ácido - Base
Aquí os dejo unos resúmenes completos con puntos claves y explicaciones de este tema. Realizados por mi en GoodNotes.
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Reacciones ácido-base
Apuntes de reacciones ácido-base de segundo de bachillerato
Termoquímica
Apuntes de termoquímica y algunos ejercicios para 2Bach
Equilibrio Químico Resumen
Resumen de elquilibro químico de 2º de bachillerato
Reacciones de transferencia de electrones. Oxidación - reducción
Apuntes de REDOX de química de 2° de bachillerato
ESQUEMA REDOX
Reacciones óxido reducción de química Preguntan mucho en EBAU
Equilibrio químico y solubilidad
Apuntes de equilibrio químico y solubilidad de química de 2° de bachillerato
Química orgánica
basicas de la química orgánica
Najpopularniji sadržaj
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
Ne možeš da nađeš ono što tražiš? Istražuj druge predmete.
Učenici nas obožavaju — i ti ćeš takođe.
Aplikacija je super laka za korišćenje i odlično dizajnirana. Našao sam sve što mi je trebalo i dosta sam naučio iz prezentacija! Definitivno ću koristiti aplikaciju za školski zadatak! A naravno, pomaže i kao inspiracija.
Ova aplikacija je stvarno odlična. Tu je toliko beleški za učenje i pomoći [...]. Na primer, problem mi je francuski, a aplikacija ima toliko opcija za pomoć. Zahvaljujući ovoj aplikaciji, poboljšao sam francuski. Preporučio bih je svima.
Vau, stvarno sam oduševljena. Probala sam aplikaciju jer sam je videla u reklamama mnogo puta i bila sam potpuno šokirana. Ova aplikacija je POMOĆ koju želiš za školu i pre svega, nudi toliko stvari, kao što su vežbe i sažeci, što mi je lično bilo VEOMA korisno.
Tendencias y Propiedades en la Tabla Periódica
¿Alguna vez te has preguntado por qué algunos elementos reaccionan violentamente y otros apenas lo hacen? La respuesta está en las propiedades periódicas, esas características que cambian de manera predecible a lo largo de la tabla periódica. Dominar estas tendencias... Prikaži više

Registruj se da vidiš sadržaj. Besplatno je!
- Pristup svim dokumentima
- Poboljšaj svoje ocene
- Pridruži se milionima učenika
Introducción a las Propiedades Periódicas
Las propiedades periódicas son las características de los elementos que varían de forma predecible en la tabla periódica. Esta periodicidad se debe a cómo se repiten las configuraciones electrónicas de la capa de valencia.
Hay dos conceptos clave que explican todo: la carga nuclear efectiva es la carga positiva "real" que siente un electrón de valencia. No es igual al número atómico porque los electrones internos "apantallan" parte de esa carga.
En un periodo (→): Z_ef aumenta porque hay más protones pero los electrones van a la misma capa. En un grupo (↓): Z_ef se mantiene casi constante para la última capa porque aunque hay más protones, también hay más capas internas que apantallan.
¡Dato clave! El efecto pantalla es como un escudo: los electrones internos protegen a los de valencia de la atracción total del núcleo.

Registruj se da vidiš sadržaj. Besplatno je!
- Pristup svim dokumentima
- Poboljšaj svoje ocene
- Pridruži se milionima učenika
Radio Atómico
El radio atómico es la mitad de la distancia entre núcleos de dos átomos idénticos enlazados. Es como medir el "tamaño" de un átomo.
En un grupo (↓): aumenta porque se añaden nuevas capas electrónicas. Cada capa nueva está más lejos del núcleo, así que el átomo es más grande. En un periodo (→): disminuye porque aunque el número de capas es el mismo, la Z_ef aumenta y "tira" más fuerte de los electrones, contrayendo el átomo.
Piénsalo así: es como si el núcleo fuera un imán que se hace más fuerte hacia la derecha (mismo periodo) pero más débil hacia abajo (mismo grupo) debido a la distancia.
Truco para recordar: Los átomos más grandes están en la esquina inferior izquierda, los más pequeños en la superior derecha.

Registruj se da vidiš sadržaj. Besplatno je!
- Pristup svim dokumentima
- Poboljšaj svoje ocene
- Pridruži se milionima učenika
Radio Iónico
Cuando un átomo gana o pierde electrones, su tamaño cambia drásticamente. Los cationes (iones positivos) son más pequeños que el átomo neutro porque al perder electrones, a menudo se pierde toda la capa de valencia y los restantes son atraídos con más fuerza.
Los aniones (iones negativos) son más grandes que el átomo neutro. Al ganar electrones en la misma capa, aumenta la repulsión entre ellos y la nube electrónica se expande.
Para especies isoelectrónicas (mismo número de electrones), a más protones en el núcleo, menor radio. Es lógico: más "tirón" hacia el centro.
Regla fácil: Perder electrones = encogerse, ganar electrones = hincharse.

Registruj se da vidiš sadržaj. Besplatno je!
- Pristup svim dokumentima
- Poboljšaj svoje ocene
- Pridruži se milionima učenika
Energía de Ionización
La energía de ionización (EI) es la energía necesaria para "arrancar" un electrón de un átomo gaseoso. Es como la fuerza que necesitas para separar algo que está pegado.
En un grupo (↓): disminuye porque los electrones están más lejos y más apantallados. En un periodo (→): aumenta porque la Z_ef aumenta y los electrones están más "pegados" al núcleo.
¡Cuidado con las excepciones! Grupo 2 vs. 13: El grupo 13 tiene EI menor porque es más fácil quitar un electrón p que uno de un orbital s completo. Grupo 15 vs. 16: El grupo 16 tiene EI menor porque elimina la repulsión de electrones emparejados.
Para examen: Aprende las excepciones de memoria. Be > B y N > O son preguntas típicas.

Registruj se da vidiš sadržaj. Besplatno je!
- Pristup svim dokumentima
- Poboljšaj svoje ocene
- Pridruži se milionima učenika
Afinidad Electrónica y Electronegatividad
La afinidad electrónica (AE) mide cuánto "le gusta" a un átomo aceptar un electrón. Si es muy negativa, significa que libera mucha energía al aceptarlo (es favorable).
En un grupo (↓): menos negativa (menos favorable) porque el electrón entrante está más lejos del núcleo. En un periodo (→): más negativa (más favorable) porque la Z_ef aumenta.
La electronegatividad es la capacidad de atraer electrones en un enlace. El flúor es el más electronegativo (4.0 en la escala de Pauling). Sigue las mismas tendencias: aumenta hacia la derecha y hacia arriba.
Dato importante: Los gases nobles tienen AE positiva - ¡no quieren electrones extra!

Registruj se da vidiš sadržaj. Besplatno je!
- Pristup svim dokumentima
- Poboljšaj svoje ocene
- Pridruži se milionima učenika
Ejemplos y Casos Prácticos
Para ordenar por radio atómico creciente: P, Cl, Na, Al (todos del periodo 3), aplicamos que el radio disminuye hacia la derecha. Resultado: Cl < P < Al < Na.
Para comparar energías de ionización entre Mg y Al, aunque Al está más a la derecha, EI(Mg) > EI(Al) por la excepción del grupo 2 vs. 13. El electrón 3p del Al es más fácil de arrancar que el 3s del Mg.
Las especies isoelectrónicas como O²⁻, F⁻, Ne, Na⁺, Mg²⁺ se ordenan por número de protones: a más protones, menor radio.
Clave del éxito: En el examen, siempre justifica con Z_ef y apantallamiento, no solo digas "aumenta hacia la derecha".

Registruj se da vidiš sadržaj. Besplatno je!
- Pristup svim dokumentima
- Poboljšaj svoje ocene
- Pridruži se milionima učenika
Resumen para Repasar
| Propiedad | Periodo (→) | Grupo (↓) | Razón |
|---|---|---|---|
| **Radio atómico** | Disminuye | Aumenta | Z_ef vs. capas nuevas |
| **Energía ionización** | Aumenta* | Disminuye | Z_ef vs. distancia+pantalla |
| **Afinidad electrónica** | Más negativa | Menos negativa | Z_ef vs. distancia+pantalla |
| **Electronegatividad** | Aumenta | Disminuye | Z_ef vs. distancia+pantalla |
*Con excepciones importantes
Lo esencial para el examen: definiciones, tendencias generales, justificaciones con Z_ef, excepciones de EI (G2 vs G13, G15 vs G16), y comparación de radios iónicos.
Consejo final: Practica con ejemplos hasta que puedas predecir propiedades sin mirar la tabla. ¡Es como tener superpoderes químicos!
Mislili smo da nikad nećeš pitati...
Šta je Knowunity AI companion?
Naš AI Companion je AI alat fokusiran na učenike koji nudi više od samih odgovora. Napravljen na milionima Knowunity resursa, pruža relevantne informacije, personalizovane planove učenja, kvizove i sadržaj direktno u chatu, prilagođavajući se tvom individualnom putu učenja.
Gde mogu da preuzmem Knowunity aplikaciju?
Možeš preuzeti aplikaciju sa Google Play Store-a i Apple App Store-a.
Da li je Knowunity stvarno besplatan?
Tako je! Uživaj u besplatnom pristupu sadržaju za učenje, povezuj se sa drugim učenicima i dobijaj trenutnu pomoć – sve na dohvat ruke.
Najpopularniji sadržaj u Química
9Ácido - Base
Aquí os dejo unos resúmenes completos con puntos claves y explicaciones de este tema. Realizados por mi en GoodNotes.
Formulación orgánica
Apuntes de formulación orgánica para 1-2 Bachillerato
Reacciones ácido-base
Apuntes de reacciones ácido-base de segundo de bachillerato
Termoquímica
Apuntes de termoquímica y algunos ejercicios para 2Bach
Equilibrio Químico Resumen
Resumen de elquilibro químico de 2º de bachillerato
Reacciones de transferencia de electrones. Oxidación - reducción
Apuntes de REDOX de química de 2° de bachillerato
ESQUEMA REDOX
Reacciones óxido reducción de química Preguntan mucho en EBAU
Equilibrio químico y solubilidad
Apuntes de equilibrio químico y solubilidad de química de 2° de bachillerato
Química orgánica
basicas de la química orgánica
Najpopularniji sadržaj
9irregular verbs quiz
Domina el idioma inglés de manera sencilla y divertida con estos flashcards diseñados especialmente para estudiantes de sexto grado.
Mesopotamia y Egipto
Contenidos sobre la civilización mesopotámica y egipcia
Grecia: Inicio de la democracia
Más o menos las preguntas que me pusieron a mí en el examen
roma
a estudiar Roma!!
Dominando la gramática inglesa: Flashcards desafiantes
Mejora tus habilidades gramaticales en inglés con estos flashcards desafiantes diseñados para estudiantes de grado 11. ¡Prepárate para dominar la gramática inglesa de manera divertida y efectiva!
Apuntes sintaxis
apuntes de sintaxis lengua 1 de bachillerato
Irregular verbs
Aprende nuevas palabras y expande tu vocabulario en inglés con esta colección de tarjetas de estudio interactivas.
filosofía
repaso filosofía "el arje , la metafísica y la crítica de Nietszche a platon"
Apuntes teorico carnet de conducir ACTUALIZADO
sacate el teorico con estos apuntes!!!
Ne možeš da nađeš ono što tražiš? Istražuj druge predmete.
Učenici nas obožavaju — i ti ćeš takođe.
Aplikacija je super laka za korišćenje i odlično dizajnirana. Našao sam sve što mi je trebalo i dosta sam naučio iz prezentacija! Definitivno ću koristiti aplikaciju za školski zadatak! A naravno, pomaže i kao inspiracija.
Ova aplikacija je stvarno odlična. Tu je toliko beleški za učenje i pomoći [...]. Na primer, problem mi je francuski, a aplikacija ima toliko opcija za pomoć. Zahvaljujući ovoj aplikaciji, poboljšao sam francuski. Preporučio bih je svima.
Vau, stvarno sam oduševljena. Probala sam aplikaciju jer sam je videla u reklamama mnogo puta i bila sam potpuno šokirana. Ova aplikacija je POMOĆ koju želiš za školu i pre svega, nudi toliko stvari, kao što su vežbe i sažeci, što mi je lično bilo VEOMA korisno.